8 mitos de las pruebas de patógenos
Publicado en:
Microbiología
Este artículo fue publicado en Spot On #3
¿Tiene curiosidad por ver qué le ofrece Spot On?
Lee ahora
Mito 1
Las pruebas de patógenos ambientales no mejoran mi programa de seguridad alimentaria
La mayoría de las normativas sobre patógenos exigen que se realicen pruebas en los productos finales antes de que un lote de producción alimentaria pueda liberarse con seguridad para su distribución y venta al por menor. Sin embargo, existen varios retos asociados a las pruebas de los productos finales. En primer lugar, variables como la microflora de fondo, las características inhibitorias, el nivel de pH y la concentración de sal dificultan la detección de patógenos. En segundo lugar, los métodos de muestreo y la heterogeneidad de las muestras pueden dar lugar a imprecisiones, especialmente si los niveles de contaminación son muy bajos. ¿Cómo pueden estar seguros los productores de alimentos de que el número de muestras analizadas es suficiente para garantizar que el lote está totalmente libre de patógenos peligrosos? Las pruebas ambientales han demostrado ser una herramienta muy útil en muchos programas de seguridad alimentaria y se han adaptado como parte de los controles preventivos en virtud de la Ley de Modernización de la Seguridad Alimentaria (FSDA) de la FDA. Los programas de vigilancia ambiental (o PGA) permiten al productor de alimentos encontrar nichos de crecimiento en las zonas de producción y tomar medidas para eliminar cualquier riesgo asociado a la contaminación de los alimentos. Las áreas con un alto riesgo de contaminación por patógenos deben ser muestreadas, ya que el propósito de las pruebas medioambientales es encontrar positivos. El objetivo de la vigilancia es erradicar los patógenos potenciales de las instalaciones y la línea de producción antes de que se produzca la contaminación real, y dar a los productores de alimentos una indicación temprana de cualquier riesgo/problema de contaminación.
Mito 2
Las pruebas internas de patógenos requieren inversiones sustanciales
Los laboratorios de servicio suelen decir a sus clientes que es demasiado caro y laborioso realizar pruebas de detección de patógenos alimentarios en sus propias instalaciones. Eso puede ser cierto si se utilizan procedimientos estándar (FDA BAM, ISO), ya que éstos suelen requerir mucho tiempo práctico. Otros métodos como el ELISA y la PCR en tiempo real requieren equipos caros. De hecho, el único equipo que necesita para las pruebas internas es una incubadora para la fase de enriquecimiento y una báscula para pesar las muestras. Un autoclave es opcional, y sólo si desea esterilizar sus propios medios o para la eliminación de residuos. También puede ser necesario disponer de una sala separada para el enriquecimiento y las pruebas. Cuando se utilizan tiras de flujo lateral, no hay necesidad de ningún equipo adicional para interpretar los resultados y, por lo tanto, no es necesaria una inversión sustancial.
Mito 3
Las pruebas de patógenos requieren personal bien formado
Los métodos rápidos para la detección de patógenos se han racionalizado desde los días en que sólo microbiólogos altamente capacitados podían administrar dichas pruebas, junto con innumerables tubos, placas y un ojo perspicaz. Todavía se requiere una serie de habilidades, dependiendo del método, pero muchos kits de pruebas pueden ser ejecutados eficazmente por personal capacitado. No todos los métodos de prueba requieren personal altamente cualificado. En muchas empresas, el personal de laboratorio puede haber sido trasladado desde la planta de producción y no tener un título científico. Por lo tanto, los métodos de prueba deben ser sencillos y sólidos, con unos pasos mínimos que ayuden a agilizar el flujo de trabajo en el laboratorio y a minimizar la posibilidad de errores. Un laboratorio también debe ser capaz de demostrar que su personal ha sido formado en el método de prueba predominante. Algunas empresas también participan en programas de pruebas de aptitud para asegurarse de que su personal de laboratorio puede trabajar de forma independiente para obtener resultados precisos de las pruebas.
Mito 4
Los requisitos de seguridad de los laboratorios disuaden a las pequeñas empresas de realizar sus propias pruebas
Los patógenos alimentarios del llamado grupo de riesgo 2, como la salmonela, la listeria y la E. coli O157, pueden manipularse en las salas con algunos ajustes menores. Los patógenos de este grupo de riesgo no se consideran peligrosos para los trabajadores de laboratorio y la comunidad en general. Según la norma europea EN 12128, Bioseguridad en los laboratorios microbiológicos y biomédicos (Centros para el Control y la Prevención de Enfermedades de EE.UU.) y el Manual de bioseguridad de la Organización Mundial de la Salud (OMS), estas salas deben estar marcadas con el símbolo de riesgo biológico y tener el acceso restringido. Sólo las personas que trabajen con los agentes patógenos deben tener acceso a esta sala de laboratorio. Las superficies de la sala deben ser resistentes a los productos químicos y, por tanto, también a los desinfectantes. Estos requisitos de seguridad del laboratorio pueden ser gestionados fácilmente por los pequeños productores de alimentos.
Mito 5
No puedo disponer del material de prueba contaminado.
Sí puedes. Aquí tienes tres opciones para una eliminación segura:
1. Utiliza un autoclave y ajusta la temperatura a 121°C durante al menos 20 minutos. Ahora el material puede ser eliminado de manera segura como residuo residual.
2. Usa un sistema de desinfección por microondas. Ahora el material puede ser eliminado de manera segura como residuo residual.
3. Delega esta tarea a una empresa de gestión de residuos. Ellos ordenarán contenedores especiales para recoger los desechos contaminados y deshacerse de ellos por ti."
Publicado en:
Microbiología
Este artículo fue publicado en Spot On #3
¿Tiene curiosidad por ver qué le ofrece Spot On?
Lee ahora
Mito 6
No es necesario seguir analizando las muestras tras un resultado positivo de la prueba
Todos los métodos rápidos disponibles en el mercado son pruebas de cribado y requieren una confirmación cultural tras un resultado "presuntamente positivo". La confirmación requiere realizar un estrechamiento de la porción enriquecida de la prueba en agares selectivos con el fin de aislar una colonia típica basándose en las características morfológicas y bioquímicas. Esto es especialmente cierto cuando se analizan productos finales o alimentos. En el caso de las muestras medioambientales, rara vez se realiza una confirmación cultural, ya que a menudo se aplican prácticas de saneamiento añadidas. Existen varias opciones de placas de agar selectivas, y las más comunes se encuentran en la Guía del laboratorio de microbiología (MLG) del USDA, el Manual de análisis bacteriológico (BAM) de la FDA o las guías de referencia ISO (véase la tabla 1).

Mito 7
No hay razón para realizar pruebas de detección de especies de Listeria cuando el adulterante es L. monocytogenes
Listeria monocytogenes (L'mono) puede ser la única cepa de Listeria regulada, pero no es la única patógena. Listeria ivanovii es otra cepa patógena que puede darse en sus instalaciones. Otra razón para realizar pruebas de Listeria spp. (todas las cepas de Listeria), especialmente en el entorno de procesamiento, es rastrear los nichos de crecimiento. Esto se debe a que L'mono puede crecer potencialmente donde prosperan otras cepas de Listeria. Es una cuestión de probabilidad que la L'mono esté presente o no. Si hay muchas cepas de Listeria no patógenas (como Listeria innocua) presentes en una muestra, podrían "sobrecrecer" L' mono en el proceso de enriquecimiento y causar potencialmente un resultado falso negativo. No es posible cultivar sólo una especie de Listeria (es decir, L'mono) durante el enriquecimiento selectivo.
Mito 8
Todos los métodos disponibles comercialmente son iguales
Hoy en día hay una plétora de métodos rápidos disponibles en el mercado y elegir entre ellos puede ser desalentador. ¿Cómo determina un productor de alimentos cuál es el mejor método para él? Todos los métodos rápidos disponibles en el mercado constan de dos partes: un enriquecimiento seguido de un paso de detección. Durante la fase de enriquecimiento se utilizan diferentes medios, ya sea un caldo convencional o uno patentado. La principal diferencia radica en el paso de detección. Los métodos de inmunoensayo detectan proteínas, mientras que los métodos de PCR detectan ADN. Deben tenerse en cuenta los siguientes criterios de evaluación: inclusividad, exclusividad, sensibilidad, especificidad, límite de detección, reproducibilidad, repetibilidad y certificación (véase la tabla 2).
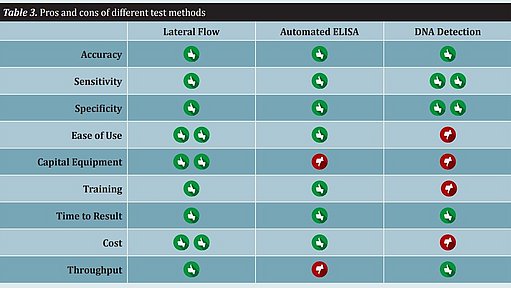
Los métodos rápidos difieren significativamente en cuanto al flujo de trabajo, la facilidad de uso y el rendimiento. Otras características de un método de ensayo que deben tenerse en cuenta son el gasto en bienes de equipo, la formación, el tiempo necesario para obtener resultados y el coste. Todos estos atributos deben tenerse en cuenta a la hora de implantar un método rápido. No existe un único método que se adapte a todos los productores de alimentos (véase el cuadro 3).