Citometría de flujo de impedancia y su uso en la vigilancia de entornos de procesamiento de alimentos
Publicado en:
Microbiología
Este artículo fue publicado en Spot On #15
¿Tiene curiosidad por ver qué le ofrece Spot On?
Lee ahora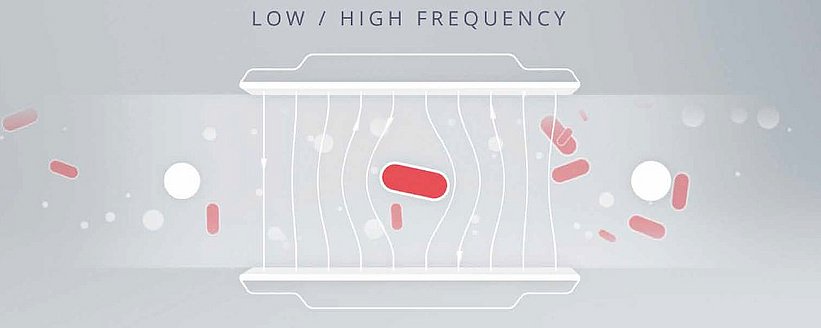
¿Qué es la citometría de flujo?
La citometría de flujo se refiere a un grupo de técnicas que utilizan un láser o un campo eléctrico para contar las células suspendidas en un fluido y determinar algunas de sus propiedades físicas o químicas. En condiciones óptimas, sólo una célula a la vez fluye a través del canal microfluídico del citómetro, que detecta las variaciones en la longitud de onda de la luz o en la carga eléctrica al paso de cada célula u otras partículas. Dado que la citometría de flujo requiere generalmente dispositivos grandes y costosos, así como fastidiosos pasos preparatorios, el método se ha limitado tradicionalmente al uso en laboratorio en campos de aplicación como la investigación y la medicina.
Publicado en:
Microbiología
Este artículo fue publicado en Spot On #15
¿Tiene curiosidad por ver qué le ofrece Spot On?
Lee ahora
Desplegar la citometría de flujo por impedancia para contar tanto células como partículas residuales
La citometría de flujo por impedancia se deriva de la tecnología en la que se basan los contadores de partículas Coulter, que pueden dimensionar y contar partículas suspendidas en electrolitos basándose en los cambios de impedancia provocados por el desplazamiento de los electrolitos por las partículas. Al medir múltiples frecuencias al mismo tiempo para cada partícula que pasa, la citometría de flujo por impedancia puede discriminar entre partículas basándose no sólo en el tamaño, sino también en las propiedades eléctricas. Se trata de una potente variante de la citometría de flujo, ya que es muy robusta y puede utilizarse para evaluar características celulares que de otro modo serían imposibles de medir sin el uso de etiquetas moleculares, como la integridad de la membrana celular. Por lo tanto, en lugar de un láser, un citómetro de flujo de impedancia emplea una corriente alterna, cuyas frecuencias variables permiten al dispositivo detectar, medir el tamaño y contar por separado las células con membrana intacta y otras partículas. En comparación con otros dispositivos de citometría de flujo, los citómetros de flujo de impedancia pueden ser ligeros, portátiles y funcionar con pilas, lo que permite utilizarlos allí donde se tome la muestra.

¿Cómo diferencian los citómetros de flujo de impedancia las células de otras partículas?
La citometría de flujo por impedancia aprovecha las propiedades electromagnéticas únicas de la membrana celular y el citoplasma para distinguir las bacterias de otras partículas. La membrana y el citoplasma de una célula influyen en el campo eléctrico de un modo diferente al de otras partículas de la muestra. Un ejemplo en el que se utilicen partículas metálicas (conductoras), partículas no conductoras y células intactas puede ilustrar este principio con mayor claridad. Independientemente de la frecuencia del campo eléctrico, la conductividad de las partículas metálicas permitirá que el campo eléctrico las atraviese sin obstáculos. Por el contrario, las partículas no conductoras, como el poliestireno, se resistirán al campo eléctrico; la corriente sólo avanzará en el medio líquido, lo que provoca un desplazamiento de volumen medible correlativo de las partículas en el canal de flujo. Las células intactas, sin embargo, son únicas en el sentido de que se asemejan tanto a partículas no conductoras como metálicas, dependiendo de la frecuencia del campo eléctrico. A bajas frecuencias, la cualidad aislante de la membrana de una célula impide que el campo eléctrico penetre en ella, lo que provoca el mismo tipo de desplazamiento que con las partículas no conductoras. Las frecuencias más altas, sin embargo, pueden penetrar parcialmente la membrana; como tales, las células son similares en conductividad a las partículas metálicas. Los microelectrodos de los citómetros de flujo de impedancia generan campos tanto a bajas como a altas frecuencias, lo que permite al dispositivo detectar estos cambios en la conductividad y la resistencia y atribuirlos en cantidades precisas a células intactas o a otras partículas. El detector identifica el objetivo como una bacteria basándose en el grado variable de impedancia o conductividad a estas frecuencias. El usuario recibe entonces recuentos separados de células intactas y de otras partículas.

¿Cómo se compara la citometría de flujo por impedancia con los métodos culturales?
Los métodos culturales, el uso de placas de agar en particular, son el enfoque tradicional para controlar la salubridad de los entornos de procesamiento de alimentos. Sin embargo, los métodos culturales, aunque bien establecidos, presentan varias desventajas en cuanto a su rapidez y alcance. Los métodos culturales son lentos, ya que requieren entre uno y diez días para que las bacterias crezcan hasta formar colonias contables. Estos métodos sólo miden lo que es cultivable en las condiciones específicas de una prueba determinada; una especie u otra agrupación de bacterias puede requerir un agar o medio líquido específico a una temperatura, grado de luz o humedad exactos, por nombrar sólo algunas variables. Los métodos de cultivo tampoco pueden pretender realizar una medición exhaustiva de todas las bacterias de una muestra. La "gran anomalía del recuento en placa", un enigma bien conocido en microbiología, observa que sólo una pequeña fracción de las bacterias de un hábitat puede recuperarse mediante cultivo. Las bacterias en estado viable pero no cultivable (VBNC) están vivas, pero debido al estrés, la idiosincrasia o factores ambientales menos que óptimos no pueden crecer en agar o en medios líquidos. En algunos casos, pueden cultivarse tras la reanimación, un proceso que, de nuevo, requiere mucho tiempo. Se sabe que algunas bacterias patógenas, como la E. coli O157, entran en estado VBNC sólo para proliferar en etapas posteriores de la cadena alimentaria o en huéspedes humanos tras su ingestión.Además, las bacterias anaerobias y microaerofílicas requieren la ausencia de oxígeno o niveles de oxígeno inferiores a los de las condiciones atmosféricas normales, respectivamente. Las bacterias de estos grupos que son cultivables requieren condiciones de incubación especiales, lo que aumenta el coste de las pruebas analíticas. Los citómetros de flujo por impedancia cuentan todas las bacterias que pasan por el canal de flujo, independientemente de su estado (cultivables, VBNC, no cultivables, latentes) o de sus requisitos de crecimiento. Esta cuantificación directa e inmediata amplía el alcance de un programa de control de la higiene; las bacterias que no se multiplican hasta que entran en contacto con los alimentos o los huéspedes potenciales también pueden ser objeto de la citometría de flujo por impedancia. También permite tomar medidas inmediatas siempre que la limpieza y la desinfección no vayan según lo previsto.