Cómo desarrollar un método multimicotoxina basado en LC-MS/MS
Publicado en:
Micotoxinas
Este artículo fue publicado en Spot On #5
¿Tiene curiosidad por ver qué le ofrece Spot On?
Lee ahora
Con frecuencia, los cultivos de cereales y las materias primas están contaminados con más de una micotoxina. Los laboratorios Romer están desarrollando un único método que puede detectar varias micotoxinas simultáneamente. Irene Hahn describe cómo.
Existen aproximadamente 400 compuestos de bajo peso molecular reconocidos como micotoxinas, cada uno con diferentes efectos tóxicos para los seres humanos y los animales. El elevado número de posibles contaminantes, así como los repetidos informes sobre la co-ocurrencia de micotoxinas, hace necesario desarrollar métodos de detección adecuados, como los métodos multimicotoxina basados en cromatografía líquida - espectrometría de masas (LC-MS/MS), para analizar simultáneamente varias micotoxinas. El desarrollo de tales métodos es todo un reto, ya que la inclusión de varias toxinas con propiedades químicas diferentes en un mismo análisis obliga a hacer concesiones a la hora de elegir los parámetros óptimos del método.
Publicado en:
Micotoxinas
Este artículo fue publicado en Spot On #5
¿Tiene curiosidad por ver qué le ofrece Spot On?
Lee ahora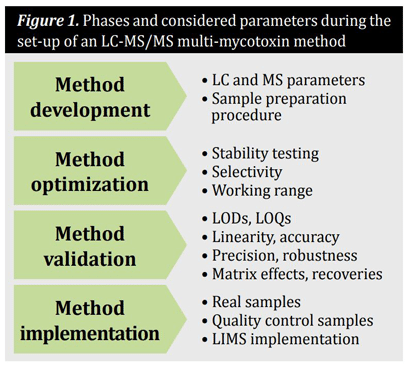
Análisis de micotoxinas basado en LC-MS/MS
Los métodos analíticos basados en LC de fase inversa acoplada a MS (LC-MS/MS) se han convertido en la última década en una técnica potente y puntera en el análisis cualitativo y cuantitativo de micotoxinas. Las ventajas de este método son la alta sensibilidad y selectividad, la aplicación al análisis de múltiples micotoxinas, así como la obtención de información adicional sobre las relaciones masa-carga (m/z) y los iones fragmento de los analitos investigados. En la actualidad, existe una fuerte tendencia hacia la aplicación de métodos multimicotoxina conseguidos mediante LC-MS/MS. Con esta técnica se puede lograr la determinación simultánea de una amplia gama de micotoxinas pertenecientes a diferentes familias químicas en una sola medición. Sin embargo, cuestiones como la diversidad química de los propios compuestos, la amplia gama de productos agrícolas que se analizan, los distintos rangos de concentración y las diferentes distribuciones de aparición suponen un reto para el desarrollo y la optimización de los métodos. Por lo tanto, hay que hacer concesiones en la elección del disolvente de extracción y la fase móvil, y las condiciones pueden estar lejos de ser óptimas para determinados analitos, que incluyen compuestos ácidos (fumonisinas), básicos (alcaloides del cornezuelo de centeno), así como polares (moniliformina, nivalenol) y apolares (zearalenona, beauvericina). Además, la falta de normas analíticas adecuadas disponibles en el mercado para determinados analitos da lugar únicamente a declaraciones de detección cualitativas en lugar de a resultados cuantitativos.
Desarrollo de un método LC-MS/MS multimicotoxina
En general, los métodos para la cuantificación de micotoxinas en cereales y productos a base de cereales se componen de un muestreo representativo, el procedimiento optimizado de preparación de la muestra y un paso de limpieza, así como la técnica analítica que incluye la separación y la detección.La puesta a punto de un método multimicotoxina basado en LC-MS/MS sigue normalmente un proceso de cuatro fases. Éstas y los parámetros considerados se resumen en la figura 1. Durante el desarrollo y la optimización del método, los parámetros influyen significativamente en la calidad y la fiabilidad de los resultados y deben evaluarse cuidadosamente. Para ello, deben utilizarse patrones analíticos de cada compuesto con la pureza indicada. Sin embargo, para determinados analitos, los estándares analíticos no están disponibles comercialmente. En esos casos, puede ser posible acceder a estándares que aún están en fase de investigación, o trabajar con material disponible que esté peor caracterizado.

Desarrollo del método
Durante el desarrollo de un método basado en LC-MS/MS, deben elaborarse los parámetros de MS y LC, así como el procedimiento de preparación de la muestra. Para la optimización de los parámetros de EM, cada compuesto debe inyectarse como patrón analítico puro directamente en el espectrómetro de masas. Posteriormente, deben evaluarse el modo de idealización (positivo o negativo), los iones precursores y de producto más abundantes, así como los potenciales de declusión ideales, las energías de colisión y los potenciales de salida de la celda de colisión. Durante la optimización de los parámetros de LC, deben evaluarse las fases móviles y el gradiente ideales, así como la columna cromatográfica óptima. El método de elección para el procedimiento de preparación de la muestra cuando se analizan múltiples micotoxinas es un enfoque de diluir y disparar sin ninguna limpieza de la muestra para no adulterar el patrón de micotoxinas durante la preparación de la muestra. Por ejemplo, rara vez se dispone de una limpieza (por ejemplo, extracción en fase sólida) que no suprima ninguno de los analitos requeridos. No obstante, si no se utiliza una limpieza, los componentes de la matriz coeluyentes e interferentes pueden afectar a la eficacia de ionización de los analitos objetivo, lo que se traduce en una peor repetibilidad y una menor precisión. Por lo tanto, la determinación y compensación de tales efectos de la matriz es esencial. Esto puede lograrse mediante la determinación de la recuperación aparente seguida de una corrección de los resultados con este valor, la calibración ajustada a la matriz o el uso de patrones internos marcados con isótopos. Esto último conducirá a resultados con la máxima precisión y fiabilidad, pero con una inversión mínima de tiempo y costes.
Optimización del método
La optimización del método analítico incluye la comprobación de la estabilidad de los analitos en la solución estándar y en las muestras, así como la comprobación de la selectividad y la determinación del intervalo de trabajo.
Validación del método
La validación del método es un requisito previo para la obtención de resultados fiables en términos de comparabilidad y trazabilidad. La validación del método debe realizarse por separado para cada analito objetivo en todas las matrices requeridas. Las características de rendimiento típicas que deben evaluarse durante la validación de un método cuantitativo son los límites de detección (LOD), los límites de cuantificación (LOQ), la linealidad, la precisión, la selectividad, la robustez, la exactitud, los efectos de la matriz y las recuperaciones. La validación del método puede realizarse añadiendo muestras en blanco con cada analito requerido en un rango de concentraciones por repetición. Cuando esté disponible, la veracidad del método debe confirmarse utilizando materiales de referencia certificados. Además, los materiales de matriz coincidente y la participación en ensayos de aptitud permiten una garantía de calidad adicional. Entre otras cosas, el número limitado de materiales de referencia es responsable del carácter semicuantitativo de estos métodos de cribado. Aunque los métodos multitoxina ya se aplican en los análisis rutinarios, deben tenerse en cuenta los elevados costes de inversión y mantenimiento.
Aplicación del método
Durante la implementación, las muestras reales, así como las muestras de control de calidad, deben medirse con el método validado. Además, el método validado debe implantarse y utilizarse en laboratorios de rutina, lo que puede resultar difícil en términos de disponibilidad de personal de laboratorio e instrumentación.
Retos generales para la determinación de micotoxinas
Normalmente, las contaminaciones por micotoxinas se distribuyen de forma heterogénea en los cultivos agrícolas y pueden concentrarse en "puntos calientes". Por lo tanto, el muestreo representa un paso importante y crucial, ya que una muestra representativa es esencial para la determinación precisa y exacta de los niveles de micotoxinas. Con la mayoría de las técnicas analíticas no se puede lograr una detección directa de las micotoxinas en las muestras de cereales molidos, por lo que se requieren procedimientos de preparación de las muestras.
Otro paso importante es la extracción de la muestra. Durante una extracción sólido-líquido convencional, las micotoxinas se extraen de las muestras de cereales molidos mediante agitación mecánica con diferentes mezclas de disolventes (acuosos y orgánicos), a veces también con modificadores ácidos o alcalinos. Los extractos resultantes pueden utilizarse posteriormente para su análisis. La mayoría de los métodos analíticos desarrollados con fines normativos y científicos se basan en la separación cromatográfica, principalmente la cromatografía líquida (CL), en combinación con diversos detectores. Los detectores de CL para el control y la detección continuos de los analitos que eluyen de la columna cromatográfica se basan en mediciones de UV/Vis-absorbancia, fluorescencia y espectrometría de masas (EM). Debido a las diferentes propiedades químicas y fisicoquímicas de las micotoxinas, la mayoría de estos métodos analíticos se han optimizado para un compuesto diana o, en el mejor de los casos, para un grupo de micotoxinas estrechamente relacionadas. Además, estos métodos dirigidos suelen incluir pasos de extracción y limpieza para reducir o eliminar los componentes no deseados de la matriz. Por lo tanto, la estimación de la presencia generada depende siempre de las muestras analizadas, así como de las micotoxinas cubiertas con los métodos analíticos utilizados.
Conclusión
En conclusión, el desarrollo de un método multimicotoxina basado en LC-MS/MS supone un reto cuando se pretende conseguir datos cuantitativos fiables y comparables. Debe considerarse cuidadosamente un gran número de parámetros diferentes que influyen significativamente en la calidad y fiabilidad de los resultados para cada analito en cada matriz por separado. Además, la diversidad química de las micotoxinas obliga a hacer concesiones durante el desarrollo del método, que pueden estar lejos de ser óptimas para determinados analitos. Por otra parte, la amplia gama de productos agrícolas, así como los distintos rangos de concentración y las diferentes distribuciones de aparición, suponen un reto adicional para el desarrollo y la optimización de los métodos. No obstante, el desarrollo de métodos multimicotoxina es ciertamente necesario y los avances en esta tecnología ampliarán aún más su aplicación.