8 mitos sobre os testes de agentes patogénicos
Publicado em:
Microbiologia
Este artigo foi publicado na Spot On #3
Está curioso para ver o que o Spot On tem para oferecer?
Leia agora
Mito 1
Os testes ambientais de agentes patogénicos não estão a melhorar o meu programa de segurança alimentar
A maioria dos regulamentos relativos a agentes patogénicos requerem o teste do produto final antes de um lote de produção alimentar poder ser libertado em segurança para distribuição e venda a retalho. No entanto, existem vários desafios associados ao teste de produtos finais. Em primeiro lugar, variáveis como a microflora de fundo, características inibitórias, nível de pH e concentração de sal dificultam a deteção de agentes patogénicos. Em segundo lugar, os métodos de amostragem e a heterogeneidade das amostras podem levar a imprecisões, especialmente se os níveis de contaminação forem muito baixos. Como podem os produtores de alimentos ter a certeza de que o número de amostras testadas é suficiente para garantir que o lote está totalmente livre de agentes patogénicos perigosos? Os testes ambientais provaram ser uma ferramenta muito útil em muitos programas de segurança alimentar e foram adaptados como parte dos controlos preventivos ao abrigo da Lei de Modernização da Segurança Alimentar da FDA (FSDA). Os programas de monitorização ambiental (ou PMAs) permitem que um produtor de alimentos encontre nichos de crescimento nas áreas de produção e tome medidas para eliminar qualquer risco associado à contaminação dos alimentos. As áreas com um elevado risco de contaminação por agentes patogénicos devem ser amostradas, uma vez que o objetivo dos testes ambientais é encontrar resultados positivos. O objetivo da monitorização é erradicar potenciais agentes patogénicos das instalações e da linha de produção antes que ocorra a contaminação real e dar aos produtores de alimentos uma indicação precoce de qualquer risco/problema de contaminação.
Mito 2
Os testes internos de agentes patogénicos requerem investimentos substanciais
Os laboratórios de serviço dizem frequentemente aos clientes que é demasiado caro e trabalhoso testar os agentes patogénicos alimentares nas suas próprias instalações. Isto pode ser verdade se forem utilizados procedimentos padrão (FDA BAM, ISO), uma vez que estes geralmente requerem muito tempo de trabalho. Outros métodos, como o ELISA e a PCR em tempo real, requerem equipamento dispendioso. De facto, o único equipamento de que necessita para testes internos é uma incubadora para a fase de enriquecimento e uma balança para pesar as amostras. Um autoclave é opcional, e apenas se desejar esterilizar os seus próprios meios ou para a eliminação de resíduos. Poderá também ser necessário dispor de uma sala separada para o enriquecimento e para os testes. Quando utiliza tiras de fluxo lateral, não necessita de qualquer equipamento adicional para interpretar os resultados, pelo que não é necessário um investimento substancial.
Mito 3
O teste de agentes patogénicos requer pessoal bem treinado
Os métodos rápidos para deteção de agentes patogénicos foram simplificados desde os dias em que apenas microbiologistas altamente qualificados podiam administrar esses testes, juntamente com inúmeros tubos, placas e um olho perspicaz. Dependendo do método, são ainda necessários vários conjuntos de competências, mas muitos kits de teste podem ser executados eficazmente por pessoal com formação. Nem todos os métodos de teste requerem pessoal altamente qualificado. Em muitas empresas, o pessoal de laboratório pode ter sido transferido da unidade de produção e pode não ter um diploma científico. Os métodos de ensaio devem, por isso, ser simples e robustos, com um mínimo de passos para ajudar a otimizar o fluxo de trabalho no laboratório e minimizar a possibilidade de erros. Um laboratório deve também ser capaz de demonstrar que o seu pessoal foi formado no método de ensaio em vigor. Algumas empresas também participam em programas de testes de proficiência para garantir que o seu pessoal de laboratório pode trabalhar de forma independente para obter resultados de teste exactos.
Mito 4
Os requisitos de segurança do laboratório impedem as pequenas empresas de efectuarem os seus próprios testes
Os agentes patogénicos alimentares do chamado grupo de risco 2, tais como Salmonella, Listeria e E.coli O157, podem ser manuseados em salas com alguns pequenos ajustes. Os agentes patogénicos deste grupo de risco não são considerados perigosos para os trabalhadores do laboratório e para a comunidade em geral. De acordo com a EN 12128 (Norma Europeia), Biossegurança em Laboratórios Microbiológicos e Biomédicos (Centros de Controlo e Prevenção de Doenças dos EUA) e o Manual de Biossegurança da Organização Mundial de Saúde (OMS), estas salas devem ser marcadas com o símbolo de risco biológico e ter acesso restrito. Apenas as pessoas que trabalham com os agentes patogénicos devem ter acesso a esta sala de laboratório. As superfícies da sala têm de ser resistentes a produtos químicos e, por conseguinte, também a desinfectantes. Estes requisitos de segurança do laboratório podem ser facilmente geridos por pequenos produtores de alimentos.
Mito 5
Não posso deitar fora o material de teste contaminado
Sim, pode. Aqui tem três opções para uma eliminação segura: 1. Utilize um autoclave e regule a temperatura para 121°C durante, pelo menos, 20 minutos. O material pode agora ser eliminado de forma segura como resíduo. 2. Utilize um sistema de desinfeção por micro-ondas. O material pode agora ser eliminado em segurança como resíduo residual. 3. Delegue essa tarefa a uma empresa de resíduos. Esta encomendará contentores especiais para recolher os resíduos contaminados e eliminá-los por si.
Publicado em:
Microbiologia
Este artigo foi publicado na Spot On #3
Está curioso para ver o que o Spot On tem para oferecer?
Leia agora
Mito 6
Não há necessidade de analisar mais amostras após um resultado de teste positivo
Todos os métodos rápidos disponíveis no mercado são testes de despistagem e requerem confirmação cultural após um resultado de teste "presumivelmente positivo". A confirmação requer a colocação da porção de teste enriquecida em ágares selectivos para isolar uma colónia típica com base nas características morfológicas e bioquímicas. Isto é especialmente verdadeiro quando se testam produtos finais ou géneros alimentícios. No caso de amostras ambientais, a confirmação cultural é raramente efectuada, uma vez que são frequentemente aplicadas práticas de saneamento adicionais. Existem várias opções de placas de ágar selectivas, sendo as mais comuns as que se encontram no Microbiology Laboratory Guidebook (MLG) do USDA, no Bacteriological Analytical Manual (BAM) da FDA ou nos guias de referência da ISO (ver Quadro 1).

Mito 7
Não há razão para testar as espécies de Listeria quando a L. monocytogenes é o adulterante
A Listeria monocytogenes (L'mono) pode ser a única estirpe de Listeria regulamentada, mas não é a única patogénica. A Listeria ivanovii é outra estirpe patogénica que pode ocorrer nas suas instalações. Outra razão para testar a Listeria spp. (todas as estirpes de Listeria), especialmente no ambiente de processamento, é seguir os nichos de crescimento. Isto porque a L'mono pode potencialmente crescer onde outras estirpes de Listeria se desenvolvem. É uma questão de probabilidade se a L'mono está presente ou não. Se muitas estirpes de Listeria não patogénicas (tais como Listeria innocua) estiverem presentes numa amostra, podem "crescer demasiado" L' mono no processo de enriquecimento e potencialmente causar um resultado falso negativo. Não é possível cultivar apenas uma espécie de Listeria (i.e., L'mono) durante o enriquecimento seletivo.
Mito 8
Todos os métodos disponíveis no mercado são iguais
Existe uma grande quantidade de métodos rápidos disponíveis no mercado atualmente e escolher entre eles pode ser assustador. Como é que um produtor de alimentos determina qual o melhor método para si? Todos os métodos rápidos disponíveis no mercado consistem em duas partes - um enriquecimento seguido de uma etapa de deteção. Durante a fase de enriquecimento são utilizados diferentes meios, quer seja um caldo convencional ou um caldo patenteado. A principal diferença reside na fase de deteção. Os métodos de imunoensaio detectam proteínas, enquanto os métodos de PCR detectam ADN. Devem ser considerados os seguintes critérios de avaliação: inclusividade, exclusividade, sensibilidade, especificidade, limite de deteção, reprodutibilidade, repetibilidade e certificação (ver Quadro 2).
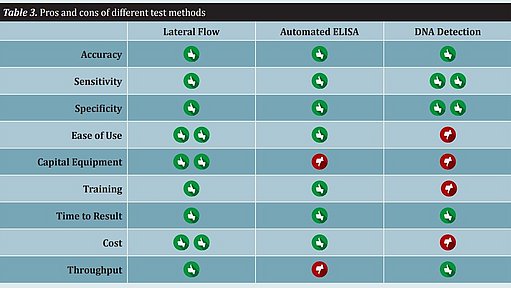
Os métodos rápidos diferem significativamente no que respeita ao fluxo de trabalho, à facilidade de utilização e ao rendimento. Entre as outras características de um método de ensaio que devem ser consideradas, contam-se as despesas com equipamento, a formação, o tempo de obtenção de resultados e o custo. Todos estes atributos devem ser tidos em consideração aquando da implementação de um método rápido. Não existe um método único que se adapte a todos os produtores de géneros alimentícios (ver Quadro 3).