Como desenvolver um método multi-micotoxinas baseado em LC-MS/MS
Publicado em:
Micotoxina
Este artigo foi publicado na Spot On #5
Está curioso para ver o que o Spot On tem para oferecer?
Leia agora
Frequentemente, as culturas de cereais e as matérias-primas estão contaminadas com mais do que uma micotoxina. A Romer Labs está a desenvolver um método único que pode detetar várias micotoxinas simultaneamente. Irene Hahn descreve como.
Existem aproximadamente 400 compostos de baixo peso molecular que são reconhecidos como micotoxinas, cada um com diferentes efeitos tóxicos para humanos e animais. O elevado número de possíveis contaminantes, bem como os repetidos relatos de coocorrência de micotoxinas, torna necessário o desenvolvimento de métodos de deteção adequados, como os métodos multi-micotoxinas baseados na cromatografia líquida - espetrometria de massa (LC-MS/MS), para analisar simultaneamente várias micotoxinas. O desenvolvimento de tais métodos é um desafio porque a inclusão de múltiplas toxinas com diferentes propriedades químicas numa análise significa que devem ser feitas concessões ao escolher os parâmetros óptimos do método.
Publicado em:
Micotoxina
Este artigo foi publicado na Spot On #5
Está curioso para ver o que o Spot On tem para oferecer?
Leia agora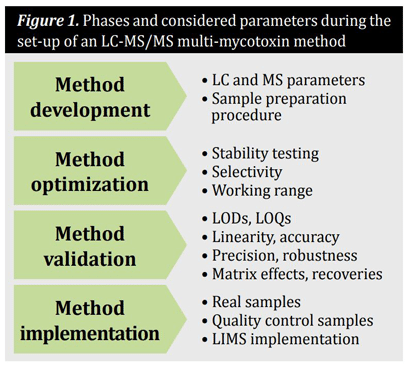
Análise de micotoxinas com base em LC-MS/MS
Na última década, os métodos analíticos baseados em LC de fase reversa acoplado a MS (LC-MS/MS) tornaram-se uma técnica poderosa e de ponta na análise qualitativa e quantitativa de micotoxinas. As vantagens deste método são a elevada sensibilidade e seletividade, a aplicação à análise de várias micotoxinas, bem como o fornecimento de informações adicionais sobre as relações massa/carga (m/z) e os iões de fragmento dos analitos investigados. Atualmente, existe uma forte tendência para a aplicação de métodos multi-micotoxinas obtidos por LC-MS/MS. Esta técnica permite a determinação simultânea de uma vasta gama de micotoxinas pertencentes a diferentes famílias químicas numa única medição. No entanto, questões como a diversidade química dos próprios compostos, a vasta gama de produtos agrícolas a testar, as gamas de concentração variáveis e as diferentes distribuições de ocorrência constituem um desafio ao desenvolvimento e otimização dos métodos. Por conseguinte, é necessário fazer concessões na escolha do solvente de extração e da fase móvel, e as condições podem estar longe de ser óptimas para determinados analitos, que incluem compostos ácidos (fumonisinas), básicos (alcalóides da cravagem do centeio), bem como compostos polares (moniliformina, nivalenol) e apolares (zearalenona, beauvericina). Além disso, a falta de padrões analíticos adequados disponíveis comercialmente para certos analitos resulta apenas em declarações de rastreio qualitativas em vez de resultados quantitativos.
Desenvolvimento de um método LC-MS/MS para multimicotoxinas
Em geral, os métodos para a quantificação de micotoxinas em cereais e produtos à base de cereais são compostos por uma amostragem representativa, o procedimento optimizado de preparação da amostra e uma fase de limpeza, bem como a técnica analítica, incluindo a separação e a deteção. Estes e os parâmetros considerados estão resumidos na Figura 1. Durante o desenvolvimento e a otimização do método, os parâmetros influenciam significativamente a qualidade e a fiabilidade dos resultados e devem ser avaliados cuidadosamente. Para este efeito, devem ser utilizados padrões analíticos de cada composto com a pureza indicada. No entanto, para certas substâncias a analisar, os padrões analíticos não estão comercialmente disponíveis. Nesses casos, poderá ser possível aceder a padrões que ainda estão a ser investigados ou trabalhar com material disponível que esteja menos bem caracterizado.

Desenvolvimento do método
Durante o desenvolvimento de um método baseado em LC-MS/MS, devem ser definidos os parâmetros de MS e LC, bem como o procedimento de preparação da amostra. Para a otimização dos parâmetros MS, cada composto deve ser injetado como um padrão analítico puro diretamente no espetrómetro de massa. Subsequentemente, devem ser avaliados o modo de idealização (positivo ou negativo), os iões precursores e os iões produto mais abundantes, bem como os potenciais ideais de declusão, as energias de colisão e os potenciais de saída da célula de colisão. Durante a otimização dos parâmetros de LC, devem ser avaliadas as fases móveis e o gradiente ideais, bem como a coluna cromatográfica ideal. O método de eleição para o procedimento de preparação da amostra quando se analisam várias micotoxinas é uma abordagem de diluir e disparar sem qualquer limpeza da amostra, de modo a não adulterar o padrão de micotoxinas durante a preparação da amostra. Por exemplo, raramente está disponível uma limpeza (por exemplo, extração em fase sólida) que não suprima nenhum dos analitos necessários. No entanto, se não for utilizada uma limpeza, os componentes da matriz co-eluentes e interferentes podem afetar a eficiência de ionização dos analitos alvo, resultando numa menor repetibilidade e precisão. Por conseguinte, é essencial determinar e compensar esses efeitos da matriz. Isto pode ser conseguido através da determinação da recuperação aparente, seguida de uma correção dos resultados com este valor, de uma calibração em função da matriz ou da utilização de padrões internos marcados com isótopos. Este último método conduzirá a resultados com a maior precisão e fiabilidade, mas com um investimento mínimo de tempo e custos.
Otimização do método
A otimização do método analítico inclui o teste de estabilidade dos analitos na solução padrão e nas amostras, bem como a prova de seletividade e a determinação do intervalo de trabalho.
Validação do método
A validação do método é um pré-requisito para a produção de resultados fiáveis em termos de comparabilidade e rastreabilidade. A validação do método deve ser efectuada separadamente para cada analito alvo em todas as matrizes necessárias. As características típicas de desempenho que devem ser avaliadas durante a validação de um método quantitativo são os limites de deteção (LOD), os limites de quantificação (LOQ), a linearidade, a precisão, a seletividade, a robustez, a exatidão, os efeitos de matriz e as recuperações. A validação do método pode ser efectuada através da adição de amostras em branco com cada analito necessário numa gama de concentrações em réplicas. Quando disponível, a exatidão do método deve ser confirmada utilizando materiais de referência certificados. Para além disso, os materiais de correspondência com a matriz e a participação em ensaios de proficiência permitem uma garantia de qualidade adicional. Entre outros factores, o número limitado de materiais de referência é responsável pelo carácter semi-quantitativo destes métodos de rastreio. Embora os métodos multitoxinas já estejam implementados nas análises de rotina, há que ter em conta os elevados custos de investimento e manutenção.
Implementação do método
Durante a aplicação, as amostras reais, bem como as amostras de controlo de qualidade, devem ser medidas com o método validado. Além disso, o método validado deve ser implementado e utilizado em laboratórios de rotina, o que pode ser difícil em termos de disponibilidade de pessoal de laboratório e de instrumentação.
Desafios gerais para a determinação de micotoxinas
Normalmente, as contaminações por micotoxinas estão distribuídas de forma heterogénea nas culturas agrícolas e podem concentrar-se em "pontos quentes". Por conseguinte, a amostragem representa um passo importante e crucial, uma vez que uma amostra representativa é essencial para a determinação precisa e exacta dos níveis de micotoxinas. Com a maioria das técnicas analíticas, não é possível a deteção direta de micotoxinas em amostras de cereais moídos, pelo que são necessários procedimentos de preparação da amostra.
Outro passo importante é a extração da amostra. Durante uma extração sólido-líquido convencional, as micotoxinas são extraídas de amostras de cereais moídos por agitação mecânica com diferentes misturas de solventes (aquosos e orgânicos), por vezes também com modificadores ácidos ou alcalinos. Os extractos resultantes podem depois ser utilizados para análise. A maioria dos métodos analíticos desenvolvidos para fins regulamentares e científicos baseia-se na separação cromatográfica, principalmente na cromatografia líquida (LC), em combinação com uma variedade de detectores. Os detectores de LC para a monitorização e deteção contínuas de analitos que eluem da coluna cromatográfica baseiam-se em medições de absorvância UV/Vis, fluorescência e espetrometria de massa (MS). Devido às diferentes propriedades químicas e físico-químicas das micotoxinas, a maioria destes métodos analíticos foi optimizada para um composto alvo ou, na melhor das hipóteses, para um grupo de micotoxinas estreitamente relacionadas. Além disso, estes métodos específicos incluem frequentemente etapas de extração e limpeza para reduzir ou eliminar componentes indesejáveis da matriz. Assim, a estimativa de ocorrência gerada depende sempre das amostras analisadas, bem como das micotoxinas abrangidas pelos métodos analíticos utilizados.
Conclusão
Em conclusão, o desenvolvimento de um método multi-micotoxinas baseado em LC-MS/MS é um desafio quando se pretende obter dados quantitativos fiáveis e comparáveis. Um vasto número de parâmetros diferentes que influenciam significativamente a qualidade e a fiabilidade dos resultados deve ser cuidadosamente considerado para cada analito em cada matriz separadamente. Além disso, a diversidade química das micotoxinas significa que têm de ser feitos compromissos durante o desenvolvimento do método, que podem estar longe de ser óptimos para determinados analitos. Além disso, a vasta gama de produtos agrícolas, bem como as gamas de concentração variáveis e as diferentes distribuições de ocorrência constituem um desafio adicional ao desenvolvimento e otimização de métodos. No entanto, o desenvolvimento de métodos multimicotoxinas é certamente necessário e os avanços nesta tecnologia alargarão ainda mais a sua aplicação.