8 miti sui test dei patogeni
Pubblicato il:
Microbiologia

Mito 1
I test sui patogeni ambientali non migliorano il mio programma di sicurezza alimentare
La maggior parte delle normative sui patogeni richiede il test del prodotto finale prima che un lotto di produzione alimentare possa essere rilasciato in sicurezza per la distribuzione e la vendita al dettaglio. Tuttavia, ci sono diverse sfide associate ai test sui prodotti finali. In primo luogo, variabili come la microflora di fondo, le caratteristiche inibitorie, il livello di pH e la concentrazione di sale rendono difficile il rilevamento dei patogeni. In secondo luogo, i metodi di campionamento e l'eterogeneità dei campioni possono portare a delle imprecisioni, soprattutto se i livelli di contaminazione sono molto bassi. Come possono i produttori alimentari essere sicuri che il numero di campioni analizzati sia sufficiente a garantire che il lotto sia del tutto privo di agenti patogeni pericolosi? I test ambientali si sono rivelati uno strumento molto utile in molti programmi di sicurezza alimentare e sono stati adattati come parte dei controlli preventivi nell'ambito del Food Safety Modernization Act (FSDA) della FDA. I programmi di monitoraggio ambientale (o EMP) consentono a un produttore alimentare di individuare le nicchie di crescita nelle aree di produzione e di intervenire per eliminare qualsiasi rischio associato alla contaminazione alimentare. Le aree ad alto rischio di contaminazione da patogeni devono essere campionate, poiché lo scopo dei test ambientali è quello di trovare i positivi. L'obiettivo del monitoraggio è quello di eliminare i potenziali agenti patogeni dalla struttura e dalla linea di produzione prima che si verifichi la contaminazione vera e propria, e di fornire ai produttori alimentari un'indicazione precoce di qualsiasi rischio/problema di contaminazione.
Mito 2
I test sui patogeni in-house richiedono investimenti sostanziali
I laboratori di servizi spesso dicono ai clienti che è troppo costoso e laborioso eseguire i test per i patogeni alimentari nella propria struttura. Questo potrebbe essere vero se si utilizzano le procedure standard (FDA BAM, ISO), che in genere richiedono molto tempo di lavoro. Altri metodi, come l'ELISA e la PCR in tempo reale, richiedono attrezzature costose. In realtà, le uniche attrezzature necessarie per i test interni sono un incubatore per la fase di arricchimento e una bilancia per pesare i campioni. L'autoclave è opzionale, e solo se desidera sterilizzare i propri terreni di coltura o per lo smaltimento dei rifiuti. Potrebbe anche essere necessaria una stanza separata per l'arricchimento e i test. Quando si utilizzano le strisce a flusso laterale, non c'è bisogno di alcuna apparecchiatura aggiuntiva per interpretare i risultati e quindi non è necessario un investimento sostanziale.
Mito 3
I test sui patogeni richiedono personale ben addestrato
I metodi rapidi per la ricerca di agenti patogeni sono stati semplificati rispetto ai tempi in cui solo microbiologi altamente qualificati potevano somministrare tali test, con innumerevoli provette, piastre e un occhio attento. A seconda del metodo, sono ancora necessarie diverse competenze, ma molti kit di analisi possono essere eseguiti efficacemente da personale qualificato. Non tutti i metodi di analisi richiedono un personale altamente qualificato. In molte aziende, il personale di laboratorio potrebbe essere stato trasferito dall'impianto di produzione e potrebbe non avere una laurea scientifica. I metodi di test devono quindi essere semplici e robusti, con passaggi minimi per aiutare a snellire il flusso di lavoro in laboratorio e ridurre al minimo la possibilità di errori. Un laboratorio deve anche essere in grado di dimostrare che il suo personale è stato formato sul metodo di prova prevalente. Alcune aziende partecipano anche a programmi di test di competenza per garantire che il personale del laboratorio sia in grado di lavorare in modo indipendente per ottenere risultati accurati.
Mito 4
I requisiti di sicurezza del laboratorio scoraggiano le piccole aziende dal condurre i propri test.
I patogeni alimentari del cosiddetto gruppo di rischio 2, come la Salmonella, la Listeria e l'E.coli O157, possono essere trattati nei locali con alcune piccole modifiche. Gli agenti patogeni di questo gruppo di rischio non sono considerati pericolosi per i lavoratori del laboratorio e per la comunità in generale. Secondo la norma EN 12128 (standard europeo), Biosafety in Microbiological and Biomedical Laboratories (US Centers for Disease Control and Prevention) e il Manuale di Biosicurezza dell'Organizzazione Mondiale della Sanità (OMS), questi locali devono essere contrassegnati con il simbolo di rischio biologico e l'accesso deve essere limitato. Solo le persone che lavorano con i patogeni devono avere accesso a questa stanza di laboratorio. Le superfici della stanza devono essere resistenti alle sostanze chimiche e quindi anche ai disinfettanti. Questi requisiti di sicurezza del laboratorio possono essere facilmente gestiti dai piccoli produttori alimentari.
Mito 5
Non posso smaltire il materiale di analisi contaminato
Sì, è possibile. Ecco tre opzioni per uno smaltimento sicuro: 1. Utilizzi un'autoclave e imposti la temperatura a 121°C per almeno 20 minuti. Il materiale può essere smaltito in modo sicuro come rifiuto residuo. 2. Utilizzare un sistema di disinfezione a microonde. Il materiale può essere smaltito in modo sicuro come rifiuto residuo. 3. Deleghi un'azienda di rifiuti per questo compito. Ordinerà dei contenitori speciali per raccogliere i rifiuti contaminati e smaltirli per lei.
Pubblicato il:
Microbiologia

Mito 6
Non è necessario analizzare ulteriormente i campioni dopo un risultato positivo del test.
Tutti i metodi rapidi disponibili in commercio sono test di screening e richiedono una conferma culturale dopo un risultato "presuntivamente positivo". La conferma richiede lo stripping della porzione di test arricchita su agar selettivi, al fine di isolare una colonia tipica in base alle caratteristiche morfologiche e biochimiche. Questo è particolarmente vero quando si analizzano prodotti finali o alimenti. Per i campioni ambientali, la conferma culturale viene eseguita raramente, poiché spesso vengono messe in atto pratiche di sanificazione aggiuntiva. Esistono diverse opzioni per le piastre agar selettive; le più comuni si trovano nella USDA Microbiology Laboratory Guidebook (MLG), nel FDA Bacteriological Analytical Manual (BAM) o nelle guide di riferimento ISO (vedere Tabella 1).

Mito 7
Non c'è motivo di testare le specie di Listeria quando l'adulterante è la L. monocytogenes.
La Listeria monocytogenes (L'mono) può essere l'unico ceppo di Listeria regolamentato, ma non è l'unico patogeno. La Listeria ivanovii è un altro ceppo patogeno che può essere presente nella sua struttura. Un altro motivo per testare la Listeria spp. (tutti i ceppi di Listeria), soprattutto nell'ambiente di lavorazione, è quello di tracciare le nicchie di crescita. Questo perché la L'mono può potenzialmente crescere dove prosperano altri ceppi di Listeria. La presenza o meno della L'mono è una questione di probabilità. Se in un campione sono presenti molti ceppi di Listeria non patogeni (come Listeria innocua), questi potrebbero "sovracrescere" L'mono nel processo di arricchimento e potenzialmente causare un risultato falso negativo. Non è possibile coltivare una sola specie di Listeria (cioè L'mono) durante l'arricchimento selettivo.
Mito 8
Tutti i metodi disponibili in commercio sono uguali
Esiste una pletora di metodi rapidi oggi disponibili sul mercato e la scelta tra questi può essere scoraggiante. Come fa un produttore alimentare a determinare quale sia il metodo migliore per lui? Tutti i metodi rapidi disponibili in commercio sono composti da due parti: un arricchimento seguito da una fase di rilevamento. Durante la fase di arricchimento vengono utilizzati diversi terreni di coltura, utilizzando un brodo convenzionale o proprietario. La differenza principale sta nella fase di rilevazione. I metodi di immunodosaggio rilevano le proteine, mentre i metodi di PCR rilevano il DNA. Si devono considerare i seguenti criteri di valutazione: inclusività, esclusività, sensibilità, specificità, limite di rilevamento, riproducibilità, ripetibilità e certificazione (vedere Tabella 2).
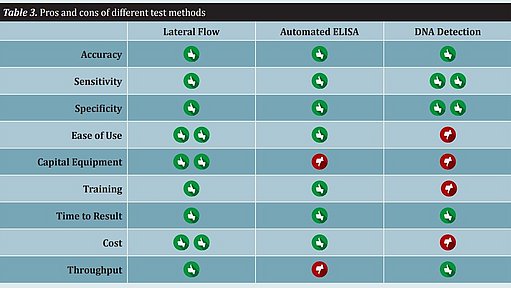
I metodi rapidi differiscono in modo significativo per quanto riguarda il flusso di lavoro, la facilità d'uso e la produttività. Diverse altre caratteristiche di un metodo di test che devono essere considerate includono la spesa per l'attrezzatura, la formazione, il tempo necessario per ottenere il risultato e il costo. Tutti questi attributi devono essere presi in considerazione quando si implementa un metodo rapido. Non esiste un unico metodo che si adatti a tutti i produttori alimentari (vedere Tabella 3).