Come sviluppare un metodo multi-micotossina basato su LC-MS/MS
Pubblicato il:
Micotossina

Spesso, i raccolti di cereali e le materie prime sono contaminati da più di una micotossina. Romer Labs sta sviluppando un unico metodo in grado di rilevare più micotossine contemporaneamente. Irene Hahn descrive come.
Esistono circa 400 composti a basso peso molecolare riconosciuti come micotossine, ciascuno con effetti tossici diversi per l'uomo e gli animali. L'elevato numero di possibili contaminanti e le ripetute segnalazioni di co-occorrenza di micotossine rendono necessario sviluppare metodi di rilevamento adeguati, come i metodi multi-micotossina basati sulla cromatografia liquida - spettrometria di massa (LC-MS/MS), per analizzare simultaneamente diverse micotossine. Lo sviluppo di tali metodi è impegnativo, perché l'inclusione di più tossine con proprietà chimiche diverse in un'unica analisi comporta la necessità di scendere a compromessi nella scelta dei parametri ottimali del metodo.
Pubblicato il:
Micotossina
Analisi delle micotossine basata su LC-MS/MS
I metodi analitici basati sulla LC in fase inversa accoppiata alla MS (LC-MS/MS) sono diventati una tecnica potente e all'avanguardia nell'analisi qualitativa e quantitativa delle micotossine nell'ultimo decennio. I vantaggi di questo metodo sono l'elevata sensibilità e selettività, l'applicazione all'analisi di più micotossine e la fornitura di informazioni aggiuntive sui rapporti massa/carica (m/z) e sugli ioni frammento degli analiti analizzati. Attualmente, c'è una forte tendenza all'applicazione di metodi multi-micotossina ottenuti mediante LC-MS/MS. Con questa tecnica si può ottenere la determinazione simultanea di un'ampia gamma di micotossine appartenenti a diverse famiglie chimiche in un'unica misurazione. Tuttavia, questioni come la diversità chimica dei composti stessi, l'ampia gamma di prodotti agricoli da analizzare, i diversi intervalli di concentrazione e le diverse distribuzioni di occorrenza rappresentano una sfida per lo sviluppo e l'ottimizzazione dei metodi. Pertanto, è necessario scendere a compromessi nella scelta del solvente di estrazione e della fase mobile, e le condizioni possono essere tutt'altro che ottimali per alcuni analiti, che includono composti acidi (fumonisine), basici (alcaloidi della segale cornuta), nonché polari (moniliformina, nivalenolo) e apolari (zearalenone, beauvericina). Inoltre, la mancanza di standard analitici adeguati e disponibili in commercio per alcuni analiti comporta solo dichiarazioni di screening qualitativo piuttosto che risultati quantitativi.
Sviluppo di un metodo LC-MS/MS multi-micotossina
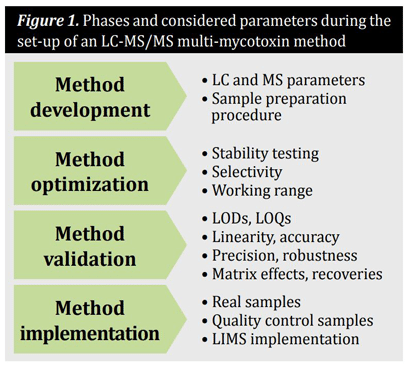
In generale, i metodi per la quantificazione delle micotossine nei cereali e nei prodotti a base di cereali comprendono un campionamento rappresentativo, una procedura di preparazione del campione ottimizzata e una fase di pulizia, nonché la tecnica analitica che include la separazione e la rilevazione. Questi e i parametri presi in considerazione sono riassunti nella Figura 1. Durante lo sviluppo e l'ottimizzazione del metodo, i parametri influenzano in modo significativo la qualità e l'affidabilità dei risultati e devono essere valutati attentamente. A tale scopo, devono essere utilizzati standard analitici di ciascun composto con purezza dichiarata. Tuttavia, per alcuni analiti, gli standard analitici non sono disponibili in commercio. In questi casi, potrebbe essere possibile accedere a standard ancora in fase di ricerca, oppure lavorare con materiale disponibile meno ben caratterizzato.

Sviluppo del metodo
Durante lo sviluppo di un metodo basato su LC-MS/MS, devono essere elaborati i parametri MS e LC, nonché la procedura di preparazione del campione. Per l'ottimizzazione dei parametri MS, ogni composto deve essere iniettato come standard analitico puro direttamente nello spettrometro di massa. Successivamente, devono essere valutati la modalità di ionizzazione ideale (positiva o negativa), gli ioni precursori e prodotti più abbondanti, nonché i potenziali di declustering ideali, le energie di collisione e i potenziali di uscita dalla cella di collisione. Durante l'ottimizzazione dei parametri LC, devono essere valutate le fasi mobili e il gradiente ideali, nonché la colonna cromatografica ottimale. Il metodo di scelta per la procedura di preparazione del campione quando si analizzano più micotossine è un approccio di diluizione e sparo senza alcuna pulizia del campione, in modo da non adulterare il modello di micotossina durante la preparazione del campione. Ad esempio, raramente è disponibile una pulizia (ad esempio, l'estrazione in fase solida) che non sopprime nessuno degli analiti richiesti. Tuttavia, se non si utilizza una pulizia, i componenti della matrice co-eluenti e interferenti possono influenzare l'efficienza di ionizzazione degli analiti target, con conseguente scarsa ripetibilità e minore accuratezza. Pertanto, la determinazione e la compensazione di tali effetti di matrice è essenziale. Ciò può essere ottenuto mediante la determinazione del recupero apparente seguita da una correzione dei risultati con questo valore, la calibrazione abbinata alla matrice o l'uso di standard interni marcati con isotopi. Quest'ultima soluzione porterà a risultati con la massima precisione e affidabilità, ma con un investimento minimo in termini di tempo e di costi.
Ottimizzazione del metodo
L'ottimizzazione del metodo analitico comprende la verifica della stabilità degli analiti nella soluzione standard e nei campioni, nonché la verifica della selettività e la determinazione dell'intervallo di lavoro.
Convalida del metodo
La validazione del metodo è un prerequisito per la produzione di risultati affidabili in termini di comparabilità e tracciabilità. La validazione del metodo deve essere eseguita separatamente per ogni analita target in tutte le matrici richieste. Le caratteristiche tipiche delle prestazioni che devono essere valutate durante la validazione di un metodo quantitativo sono i limiti di rilevazione (LOD), i limiti di quantificazione (LOQ), la linearità, la precisione, la selettività, la robustezza, l'accuratezza, gli effetti della matrice e i recuperi. La convalida del metodo può essere eseguita prelevando campioni bianchi con ogni analita richiesto ad una gamma di concentrazioni in replica. Se disponibile, l'esattezza del metodo deve essere confermata utilizzando materiali di riferimento certificati. Inoltre, i materiali abbinati alla matrice e la partecipazione a test di competenza consentono di ottenere un'ulteriore garanzia di qualità. Tra l'altro, il numero limitato di materiali di riferimento è responsabile del carattere semi-quantitativo di questi metodi di screening. Sebbene i metodi multi-tossina siano già implementati nelle analisi di routine, è necessario considerare gli elevati costi di investimento e di manutenzione.
Implementazione del metodo
Durante l'implementazione, i campioni reali e i campioni di controllo qualità devono essere misurati con il metodo convalidato. Inoltre, il metodo convalidato deve essere implementato e utilizzato nei laboratori di routine, il che può essere difficile in termini di disponibilità di personale di laboratorio e di strumentazione.
Sfide generali per la determinazione delle micotossine
Di solito, le contaminazioni da micotossine sono distribuite in modo eterogeneo nelle colture agricole e possono essere concentrate in 'punti caldi'. Pertanto, il campionamento rappresenta una fase importante e cruciale, in quanto un campione rappresentativo è essenziale per la determinazione precisa e accurata dei livelli di micotossine. Con la maggior parte delle tecniche analitiche, non è possibile ottenere una rilevazione diretta delle micotossine nei campioni di cereali macinati e quindi sono necessarie procedure di preparazione del campione.
Un'altra fase importante è l'estrazione del campione. Durante un'estrazione solido-liquido convenzionale, le micotossine vengono estratte dai campioni di cereali macinati mediante agitazione meccanica con diverse miscele di solventi (acquosi e organici), talvolta anche con modificatori acidi o alcalini. Gli estratti risultanti possono poi essere utilizzati per l'analisi. La maggior parte dei metodi analitici sviluppati per scopi normativi e scientifici si basa sulla separazione cromatografica, principalmente sulla cromatografia liquida (LC), in combinazione con una varietà di rilevatori. I rivelatori LC per il monitoraggio e il rilevamento continuo degli analiti che fuoriescono dalla colonna cromatografica si basano su misurazioni di assorbanza UV/Vis, fluorescenza e spettrometria di massa (MS). A causa delle diverse proprietà chimiche e fisico-chimiche delle micotossine, la maggior parte di questi metodi analitici sono stati ottimizzati per un composto target, o al massimo per un gruppo di micotossine strettamente correlate. Inoltre, questi metodi mirati spesso includono fasi di estrazione e pulizia per ridurre o eliminare i componenti indesiderati della matrice. Pertanto, la stima dell'occorrenza generata dipende sempre dai campioni analizzati e dalle micotossine trattate con i metodi analitici utilizzati.
Conclusione
In conclusione, lo sviluppo di un metodo multi-micotossina basato su LC-MS/MS è impegnativo quando si vuole ottenere dati quantitativi affidabili e comparabili. Un gran numero di parametri diversi che influenzano in modo significativo la qualità e l'affidabilità dei risultati deve essere considerato attentamente per ogni analita in ogni matrice separatamente. Inoltre, la diversità chimica delle micotossine comporta la necessità di scendere a compromessi durante lo sviluppo del metodo, che può essere tutt'altro che ottimale per alcuni analiti. Inoltre, l'ampia gamma di prodotti agricoli, nonché i vari intervalli di concentrazione e le diverse distribuzioni di presenza, mettono ulteriormente a dura prova lo sviluppo e l'ottimizzazione dei metodi. Tuttavia, lo sviluppo di metodi multi-micotossina è certamente necessario e i progressi di questa tecnologia ne estenderanno ulteriormente l'applicazione.