8 mitów na temat testowania patogenów
Opublikowano:
Mikrobiologia
Ten artykuł został opublikowany w Spot On #3
Są Państwo ciekawi, co Spot On ma do zaoferowania?
Proszę przeczytać teraz
Mit 1
Testowanie patogenów środowiskowych nie poprawia mojego programu bezpieczeństwa żywności
Większość przepisów dotyczących patogenów wymaga testowania produktów końcowych przed bezpiecznym dopuszczeniem partii produkcyjnej żywności do dystrybucji i sprzedaży detalicznej. Istnieje jednak kilka wyzwań związanych z testowaniem produktów końcowych. Po pierwsze, zmienne takie jak mikroflora tła, właściwości hamujące, poziom pH i stężenie soli utrudniają wykrywanie patogenów. Po drugie, metody pobierania próbek i ich niejednorodność mogą prowadzić do niedokładności, zwłaszcza jeśli poziomy zanieczyszczenia są bardzo niskie. W jaki sposób producenci żywności mogą mieć pewność, że liczba przebadanych próbek jest wystarczająca, aby zapewnić, że dana partia jest całkowicie wolna od niebezpiecznych patogenów? Testy środowiskowe okazały się bardzo przydatnym narzędziem w wielu programach bezpieczeństwa żywności i zostały zaadaptowane jako część kontroli zapobiegawczych zgodnie z ustawą FDA Food Safety Modernization Act (FSDA). Programy monitorowania środowiska (lub EMP) pozwalają producentowi żywności znaleźć nisze wzrostu w obszarach produkcyjnych i podjąć działania w celu wyeliminowania wszelkiego ryzyka związanego z zanieczyszczeniem żywności. Należy pobierać próbki z obszarów o wysokim ryzyku skażenia patogenami, ponieważ celem testów środowiskowych jest znalezienie pozytywnych wyników. Celem monitorowania jest wyeliminowanie potencjalnych patogenów z zakładu i linii produkcyjnej, zanim dojdzie do faktycznego skażenia, i zapewnienie producentom żywności wczesnego wskazania ryzyka/problemu związanego z zanieczyszczeniem.
Mit 2
Wewnętrzne testowanie patogenów wymaga znacznych inwestycji
Laboratoria usługowe często mówią klientom, że testowanie patogenów żywności we własnym zakładzie jest zbyt kosztowne i pracochłonne. Może to być prawdą, jeśli stosowane są standardowe procedury (FDA BAM, ISO), ponieważ zazwyczaj wymagają one dużo czasu. Inne metody, takie jak ELISA i PCR w czasie rzeczywistym, wymagają drogiego sprzętu. W rzeczywistości jedynym sprzętem potrzebnym do testów wewnętrznych jest inkubator do fazy wzbogacania i waga do ważenia próbek. Autoklaw jest opcjonalny i tylko wtedy, gdy chcą Państwo sterylizować własne pożywki lub usuwać odpady. Może również zaistnieć potrzeba wydzielenia osobnego pomieszczenia do wzbogacania i testowania. W przypadku korzystania z pasków bocznego przepływu nie ma potrzeby stosowania dodatkowego sprzętu do interpretacji wyników, a zatem nie jest konieczna znaczna inwestycja.
Mit 3
Testowanie patogenów wymaga dobrze wyszkolonego personelu
Szybkie metody wykrywania patogenów zostały usprawnione od czasów, gdy tylko wysoko wykwalifikowani mikrobiolodzy mogli przeprowadzać takie testy, wraz z niezliczonymi probówkami, płytkami i wnikliwym okiem. W zależności od metody nadal wymagane są różne zestawy umiejętności, ale wiele zestawów testowych może być skutecznie obsługiwanych przez przeszkolony personel. Nie wszystkie metody testowe wymagają wysoko wykwalifikowanego personelu. W wielu firmach pracownicy laboratoriów mogli zostać przeniesieni z zakładu produkcyjnego i mogą nie mieć wykształcenia naukowego. Metody testowe powinny być zatem proste i solidne, z minimalnymi krokami, aby pomóc usprawnić przepływ pracy w laboratorium i zminimalizować ryzyko błędów. Laboratorium musi również być w stanie wykazać, że jego pracownicy zostali przeszkoleni w zakresie obowiązującej metody testowej. Niektóre firmy uczestniczą również w programach testów biegłości, aby upewnić się, że ich personel laboratoryjny może pracować niezależnie w celu uzyskania dokładnych wyników testów.
Mit 4
Wymogi dotyczące bezpieczeństwa w laboratorium zniechęcają małe firmy do przeprowadzania własnych testów
Patogeny żywnościowe z tzw. grupy ryzyka 2, takie jak Salmonella, Listeria i E. coli O157, mogą być obsługiwane w pomieszczeniach z niewielkimi zmianami. Patogeny z tej grupy ryzyka nie są uważane za niebezpieczne dla pracowników laboratoriów i ogółu społeczeństwa. Zgodnie z normą EN 12128 (norma europejska), Biosafety in Microbiological and Biomedical Laboratories (US Centers for Disease Control and Prevention) oraz podręcznikiem bezpieczeństwa biologicznego Światowej Organizacji Zdrowia (WHO), takie pomieszczenia powinny być oznaczone symbolem zagrożenia biologicznego i mieć ograniczony dostęp. Tylko osoby pracujące z patogenami powinny mieć dostęp do tego pomieszczenia laboratoryjnego. Powierzchnie w pomieszczeniu muszą być odporne na chemikalia, a zatem również na środki dezynfekujące. Te wymagania dotyczące bezpieczeństwa w laboratorium mogą być łatwo spełnione przez małych producentów żywności.
Mit 5
Nie mogę pozbyć się skażonego materiału testowego
Tak, może Pan. Oto trzy opcje bezpiecznej utylizacji: 1. Proszę użyć autoklawu i ustawić temperaturę na 121°C na co najmniej 20 minut. Materiał można teraz bezpiecznie usunąć jako odpady resztkowe. 2. Proszę użyć systemu dezynfekcji mikrofalowej. Materiał można teraz bezpiecznie usunąć jako odpady resztkowe. 3. Proszę zlecić to zadanie firmie zajmującej się odpadami. Zamówi ona specjalne kontenery do zbierania skażonych odpadów i usunie je dla Państwa.
Opublikowano:
Mikrobiologia
Ten artykuł został opublikowany w Spot On #3
Są Państwo ciekawi, co Spot On ma do zaoferowania?
Proszę przeczytać teraz
Mit 6
Nie ma potrzeby dalszej analizy próbek po uzyskaniu pozytywnego wyniku testu
Wszystkie dostępne na rynku szybkie metody są testami przesiewowymi i wymagają potwierdzenia kulturowego po "przypuszczalnie pozytywnym" wyniku testu. Potwierdzenie wymaga posiewu wzbogaconej porcji testowej na agary selektywne w celu wyizolowania typowej kolonii na podstawie cech morfologicznych i biochemicznych. Jest to szczególnie ważne w przypadku testowania produktów końcowych lub środków spożywczych. W przypadku próbek środowiskowych potwierdzenie kulturowe jest rzadko wykonywane, ponieważ często stosowane są dodatkowe praktyki sanitarne. Istnieje kilka opcji selektywnych płytek agarowych, z których najpopularniejsze można znaleźć w przewodniku USDA Microbiology Laboratory Guidebook (MLG), FDA Bacteriological Analytical Manual (BAM) lub przewodnikach referencyjnych ISO (patrz Tabela 1).

Mit 7
Nie ma powodu, aby badać gatunek Listeria, gdy substancją zafałszowującą jest L. monocytogenes.
Listeria monocytogenes (L'mono) może być jedynym regulowanym szczepem Listeria, ale nie jest jedynym patogennym. Listeria ivanovii to kolejny patogenny szczep, który może występować w Państwa zakładzie. Innym powodem testowania Listeria spp. (wszystkich szczepów Listeria), zwłaszcza w środowisku przetwórczym, jest śledzenie nisz wzrostu. Wynika to z faktu, że L'mono może potencjalnie rosnąć tam, gdzie rozwijają się inne szczepy Listeria. To, czy L'mono jest obecna, czy nie, jest kwestią prawdopodobieństwa. Jeśli w próbce znajduje się wiele niepatogennych szczepów Listeria (takich jak Listeria innocua), mogą one "przerosnąć" L'mono w procesie wzbogacania i potencjalnie spowodować fałszywie ujemny wynik. Nie jest możliwe wyhodowanie tylko jednego gatunku Listeria (tj. L'mono) podczas selektywnego wzbogacania.
Mit 8
Wszystkie dostępne na rynku metody są takie same
Obecnie na rynku dostępnych jest mnóstwo szybkich metod, a wybór między nimi może być zniechęcający. W jaki sposób producent żywności może określić, która metoda jest dla niego najlepsza? Wszystkie dostępne na rynku szybkie metody składają się z dwóch części - wzbogacania, po którym następuje etap wykrywania. W fazie wzbogacania stosowane są różne pożywki, przy użyciu konwencjonalnego lub zastrzeżonego bulionu. Główna różnica polega na etapie wykrywania. Metody immunologiczne wykrywają białka, podczas gdy metody PCR wykrywają DNA. Należy wziąć pod uwagę następujące kryteria oceny: inkluzywność, ekskluzywność, czułość, specyficzność, granica wykrywalności, odtwarzalność, powtarzalność i certyfikacja (patrz Tabela 2).
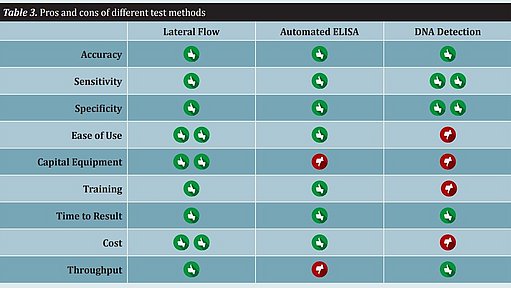
Szybkie metody różnią się znacznie pod względem przebiegu pracy, łatwości użycia i wydajności. Kilka innych cech metody testowej, które należy wziąć pod uwagę, obejmuje nakłady kapitałowe na sprzęt, szkolenie, czas uzyskania wyniku i koszt. Wszystkie te cechy należy wziąć pod uwagę przy wdrażaniu szybkiej metody. Nie ma jednej metody, która pasowałaby do wszystkich producentów żywności (patrz Tabela 3).